SVARFORUM.cz - forum o svářečkách a svařováníChcete-li přispívat do fóra, musíte se zaregistrovat ! Navštivte také: SVAR INFO |

|
Nejste přihlášen(a)
- Index - hlavní stránka
- » Svařování plamenem a řezání kyslíkem
- » Fľašový ventil + redukčný ventil PB
#76 21-01-2024 14:41:29
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Mapp je propin čili dnes propyn. Vyšší uhlovodík v řadě po acetylenu, metylacetylen. C3H4 Izomerizuje s 1,2propandienem, takže by se měl vyskytovat ve směsi metylacetylenu a 1,2propoandienu. Vře při teplotě cca -23 st C, 1,2 propandien při teplotě tuším -12 st C.
Pokud se u nás prodává v malých nádobách, tak asi není nijak zakázaný třeba zelenými předpisy a kdo si ho objedná, může ho dostat ve velkém balení. když si to zaplatí. Předpokládám, že na rozdíl od acetylénu se dá skladovat stlačený jako kapalina v bombách podobně jako PB.
Offline
#77 21-01-2024 14:48:30
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
bourač napsal(a):
Navíc v hydrokraku se nikdy nemůže podařit jednotlivé uhlovodíky oddělit, vždy to bude nějaká směs.
Můžou bez problémů oddělit i uhlovodíky s rozdílem teploty varu o desetině stupně C. Natož pak propan s teplotou varu -42,1, izobutan s teplotou varu kolem - 10 st C a butan s teplotou varu kolem 0 st C. Jenom musí někdo tu kolonu a tu energii na rozdělení chtít zaplatit. Pro topení, už kvůli ceně bude stačit to hrubé rozdělení.
Offline
#78 21-01-2024 15:18:32
Re: Fľašový ventil + redukčný ventil PB
m.evil napsal(a):
Ten MAPP vyzerá zaujímavo.
Problém je ale v tom , že u nás sa predáva len v malých nádobách do ručných horákov.
Je to nejakých 380 gramov náplne .
Bolo by super , ak by sa to dalo použiť ako náhrada acetylénu spolu s kyslíkom.
Občas potrebujem niečo nahriať no PB na to nestačí.
Tak ten MAPP jako náhrada acetylenu, co se týče bezpečnosti je OK. Ale jinak kyslík - acetylen plamen dosahuje 3200°C a ten MAPP - kyslík 2950. S propanem jen asi 2880°C... Na nahřívání, pájení i svařování je to dostatečné, ale na svařování oceli se mi to nejevilo super. Tam je acetylen nenahraditelný, neboť spaliny obsahují daleko menší podíl vodních par.
Offline
#79 21-01-2024 17:53:01
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Tsk acetylém má vzorec C2H2 plus z hlediska tepla jednu trojnou vazbu, která sama o sobě svým rozpadem uvolní značné množství tepla. MAPP má vzorec C3H4 plus k tomu ta jedná trojná vazba nebo na izomeru dvě dvojné vazby, to je vyšší objem spalin proti acetylenu v poměru 5:3 , přitom vazebné teplo z jedné trojné nebo dvou dvojných vazeb zhruba stejné.
Offline
#80 21-01-2024 22:00:13
Re: Fľašový ventil + redukčný ventil PB
Radim - Já nevím, ale nemýlíte se? MAPP Gas sám nemá chem. vzorec, především je to směs čtyř H/C.
jestli jste četl ten odkaz, co jsem dal výše, tak tam je to vcelku srozumitelně vysvětleno.
https://www.differencebetween.com/diffe … d-propane/
MAPP je pojmenován podle směsi čtyř uhlovodíků. Není tam uveden poměr H/C té směsi.
Methyl Vzorec CH3
Acetylen Vzorec: C2H2
Propadien Vzorec: C3H4
Propan Vzorec: C₃H₈
Offline
#81 22-01-2024 08:06:07
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
No, může tam vlastně být příměs propanu, už z toho důvodu, že se metylacetylen z propanu vyrábí.
Jinak ale metyl není sloučenina, ale uhlovodíkový zbytek CH3-
Acetylen je sloučenina C2H2, ale taky, když se vezme triviální název, acetylénový nebo etinový zbytek -C2H1 nebo -C=-CH (není znak pro trojnou vazbu) Neboli metylacetylen neboli 1metylacetylen je potom H3C-C=-CH neboli sumární vzorec C3H4.
propadien je potom H2C=C= CH2, kde proti metyl benzenu se přesunuje jeden vodík a potom vazební elektrony z jedné trojné vazby na dvě dvojné. Jestli dobře čtu ty hodnoty, co jsem si našel, tak za normální teploty se metylacetylen CH3-C=-CH samovolně přeměňuje na propadien H2C=C= CH2 a zpátky asi tak, že zhruba pětina objemu je propadien a zbytek je metykacetylen.
Takže by tm mohly být tři sloučeniny. je otázka, co to bude dělat při používání, když propan má teplotu varu těch -42stC, metylacetylen -24 a propadien kolem -10 st C. Při malém odběru z velké flašky bude nejdřív plyn asi málo kvalitní, protože v něm bude hodně propanu.
Offline
#82 22-01-2024 12:09:47
Re: Fľašový ventil + redukčný ventil PB
Radim - No, já jsem o tom až takto podrobně dosud nebádal, ani to takto z hlavy nemám nastudováno, spíše jsem s ním, acetylenem a propanem několik let pracoval a chtěl zde uvést praktické poznatky - mohu tudíž z praxe porovnat MAPP s acetylenem. Takže můj osobní názor - není to až tak dramatický rozdíl při nahřívání mezi použitím MAPP a propanem. Vzhlem k ceně propanu, která je asi 3x nižší, než MAPP!!! MAPP je levnější, ale hlavně bezpečnější, než acetylen, zejména při ohřevu obrovských předmětů... Když kouknu do Wikipedie, tak co tam uvádějí, bych potvrdil. - (zkrácený užitečný překlad):
Originální plyn MAPP lze použít v kombinaci s kyslíkem pro zahřívání, pájení, pájení a dokonce i svařování, protože má vysokou teplotu plamene 2925°C (5300°F) v kyslíku. Ačkoli má acetylen vyšší teplotu plamene (3160°C, 5720°F), MAPP má tu výhodu, že během přepravy nevyžaduje ředění ani speciální náplně nádob, což umožňuje přepravu většího objemu topného plynu při stejné dané hmotnosti, a při používání je mnohem bezpečnější. Plamen MAPP/kyslík není zcela vhodný pro svařování oceli, kvůli vysoké koncentraci vodíku v plameni – vyšší než acetylen, ale nižší než kterýkoli z ostatních ropných palivových plynů. Vodík proniká do roztavené oceli a činí svary křehkými. MAPP/kyslík byl s výhodou používán při řezání pod vodou, které vyžaduje vysoké tlaky plynu (pod takovými tlaky se acetylen může explozivně rozkládat, takže jeho použití je nebezpečné...
Složení dodávaného plynu se značně měnilo, přičemž plyny dodávané různými přebalovači/prodejci se v kterémkoli okamžiku měnily, stejně jako obecné složení se v průběhu času měnilo, ale typické složení pro původní plyn může být:
methylacetylen ( propin) 48 %, propadien 23 %, propan 27 %. Pro pozdější Dow/Petromont plyn propin 30%, propadien 14%, propylen 43%, propan 7%, C4H10 ( isobutan , butan ) 6 % může být typičtější.
Více podrobností zde:
https://en.wikipedia.org/wiki/MAPP_gas
Offline
#83 22-01-2024 15:41:24
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Propin nebo propyn je metylacetylen, je to jen jiný chemický název podle trochu jiného způsobu chemického názvosloví.
Obecně lineární uhlovodíky s jednoduchou vazbou jsou alkany, metan, etan, propan, butan ......
lineární uhlovodíky s jednou dvojnou vazbou jsou alkeny, eten, propen, buten, penten...., se dvěma dvojnými vazbami jsou ...dieny, propadien, butadien, pentadien
S jednou trojnoiu vazbou jsou za našich dob alkiny, dnes alkyny. , propin, butin, pentin.....
propin neboli metylacetylen se může potom taky nazývat metyletin jako třetí regulérní název.
Editoval Radim (22-01-2024 15:41:49)
Offline
#84 22-01-2024 20:34:54
- jirkati
- Moderator
- Místo: Liberec
- Registrovaný: 07-12-2007
- Příspěvky: 4653
Re: Fľašový ventil + redukčný ventil PB
To Radim - hezky popsáno, ale v tom chemickém rozboru nevidím z hlediska svařování smysl.
MAPP byl koncipován jako "náhrada" acetylénu. Čas a praxe ukázaly jeho možnosti využití na ohřev a řezání kovů. Velké množství v plamenu chemicky vznikající vodní páry brání použití ke svařování. Kolem svarové lázně je vlastně ochranná atmosféra spalin. Vodík - i z vodní páry - je nepřítelem svařování, protože přímo způsobuje kromě pórů také vodíkovou praskavost. Každý zná nutnost sušení obalovaných elektrod.
Offline
#85 22-01-2024 22:09:28
Re: Fľašový ventil + redukčný ventil PB
jirkati - Přesně zejména na toto jsem se snažil poukázat a zohlednit hlavně použitelnost. Acetylén je z tohoto hlediska nenahraditelný při svařování oceli. Škoda, že už nemám přístup na bývalé pracoviště... Vyrobil bych pár vzorků sváru plamenem za použití MAPP vs. acetylén. Kdysi jsem to předváděl ve Svářecí škole. Jednak je ta porosita při MAPP/kyslík viditelná přímo při svařování a potom u výbrusu sváru.
Offline
#86 23-01-2024 07:59:11
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Tak pro svářeče při vlastním svařování taky nemá smysl informace, že se třeba titan anebo složky celulózy z obalu v oblouku snadno ionizují a vytvářejí kolem svaru ochrannou atmosféru. Pro svářeče v okamžiku svaru je podstatné hlavně to, že to svařuje a jak dobře.
U acetylenu velkou teplotu plamene přináší energie trojné vazby. Platí nejdřív formální rovnice že acetylen se rozloží na uhlík a vodík a přitom se uvolní dost značné množství vazební energie.
C2H2 -> 2C + H2 plus vazební energie
Ta by měla, co jsem kdysi viděl v nějakých tabulkách, dosahovat až poloviny celkového spalného tepla reakce
2C + H2 -> 2 CO2 + H2O plus spalné teplo vodíku a uhlíku
Neboli při spalování acetylénu by se na jeho uhlík a vodík mělo uvolnit až 1,5 x větší množství energie než při spalování alkanů, třeba propanu nebo butanu. Protože tam je ta vazební energie zanedbatelná nebo dokonce mírně minusové, co si pamatuji, činí nějak nižší jednotky procent na spalné teplo uhlíku a vodíku obsažené v tom plynu. Proto má acetylen s kyslíkem teplotu plamene takovou a propan s kyslíkem zase jinou.
Vysoké vazební teplo trojné vazby v acetylenu způsobuje vedle jiných faktorů taky nestabilitu acetylenu při vyšších tlacích. Mikroteplo uvolněné nějakým náhodným rozkladem pár molekul acetylenu při vyšším tlaku iniciuje další rozpad molekul acetylenu v blízkém okolí a tak se rozjede řetězová reakce, kde se rozpadne všechen acetylen uvnitř v láhvi. Objem se přitom teoreticky nemění, protože určitý objem acetylenu se rozpadne na úplně stejný objem vodíku plus zanedbatelný objem tuhých sazí uhlíku. Ale rozkladem trojné vazby v molekulách acetylenu se uvolní velké množství energie, které ohřeje zplodiny rozkladu acetylenu a tím podstatně zvýší tlak v láhvi, takže se roztrhne. Výpočtem, kde by se vzalo vazebné teplo trojné vazby acetylenu a měrná tepla toho vodíku, sazí a náplně láhve by se potom dalo spočítat, na jakou teplotu ten rozklad acetylenu vnitřek láhve ohřeje a tudíž jaký asi maximální tlak by tam asi mohl nastat.
Co se týká používání metylacetylenu neboli propinu ke svařování, na spoustu věcí se nemusí čekat, až "čas a praxe" prokáže, že tomu tak je. Stačí sednout jen k papíru, nemusí to být ani k počítači a spočítat si to.
u acetylenu je vazební energie trojné vazby na dvě molekuly oxidu uhličitého a jednu molekulu vodní páry
C2H2 -> 2 CO2 + H2O
U etinu stejná vazební energie jedné trojné vazby připadá na v poměru 3:5 větší objem spalin a v poměru 106:168 na větší hmotnost spalin.
C3H4 -> 3 CO2 + 2H2O
Neboli ten přídavek energie z vazebné energie trojné vazby se u etinu příslušně rozředí a potom logicky teplota plamene vychází výrazně nižší. Ale pořád vyšší než třeba u propanu.
Totéž u ovlivnění svaru vodíkem z vodní páry. U acetylenu je v ideálních spalinách plamene s kyslíkem objemový poměr oxidu uhličitého ku vodní páře 2:1, u etinu je jen 3:2 a u propanu je 3:4.
Takže se nemusí čekat, až spousta svářečů na vlastní kůži a na vlastní peníze prokáže, že tomu tak je. Stačí si to dopředu spočítat a potom ještě případně ověřit na nějakých jednoduchých zkouškách.
Editoval Radim (23-01-2024 08:06:13)
Offline
#87 23-01-2024 12:34:53
Re: Fľašový ventil + redukčný ventil PB
Pane Radime, nezlobte se, ale to, co jste zde předvedl, je sice velice odborné, ale tak trochu zbytečné. O co se zde dohadujete? To, co zde píšete o ionizaci a titanu je přitažené za vlasy. U elektrod pro svařování má obal tyto vlastnosti a základní funkce:
Funkce plynotvorná (při hoření oblouku vznikají z obalu kouře a plyny, které vytvářejí
druh ochranné atmosféry a brání přístupu vzdušného kyslíku a dusíku ke svarové lázni,
např.celulosa, tepelný rozklad CaCO3 na CO2 a CaO ),
- funkce ionizační (slouží v obalu pro usnadnění zapalovaní a hoření oblouku, např. elektricky vodivé soli alkalických kovů K a Na).
- funkce metalurgická – rafinace (snížení P a S), desoxidace ( snížení O2 ) a legování
( především prvků náchylných k propalu – Cr,Mo,Ti atd.)
To další o vzniku tepla a všechno ostatní v podstatě nalezne pozorný čtenář v tom odkazu, co jsem dal výše, pokud si ho celý pozorně přečte. Konec konců ani to není nutné. Není potřeba pro svářeče tohle všechno detailně vědět a už vůbec na něm požadovat, aby sednul ke computeru a počítal téměř vědecké výpočty, když si v práci sedne, udělá si dva jednoduché testy a má vcelku jasno. Není nad poznání v praxi, samozřejmě s určitými vědomosti a nauce o materiálech.Ale to všechno se probírá ve Svářecích školách... Naprosto zbytečný další comment!
Ještě sem dám tabulku o vlastnostech acetylenového plamene a důvod, proč je nenahraditelný pro svařování oceli: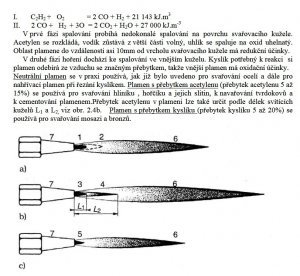
Editoval Frank (23-01-2024 12:38:31)
Offline
#88 23-01-2024 12:53:54
- Famater
- Člen
- Místo: Hradec Králové
- Registrovaný: 24-01-2012
- Příspěvky: 5036
Re: Fľašový ventil + redukčný ventil PB
Pro domácí jeden odkaz:
http://www.proferplyn.cz/?m=6
Toto mě jednou zaujalo. Protože plamenem jen pájím natvrdo propan kyslíkem tak jsem usoudil, že to je pro mne zbytečné. Tak jsem ani nezjistil jestli je to skutečně dostupné. Jinak pro chlaďaře je MAPP vynikající. Dosahují potřebné teploty na tvrdé pájení i bez kyslíku.
TP1500, KITin 170LA, JLT250 ACDC,vodní chlazení vl. výroby, hořák SR18, Binzel SR26 s pot., Plasma CUT55, autogen PB-kyslík
Křemíková 3fáz 200A vl. konstrukce
Offline
#89 23-01-2024 13:18:32
Re: Fľašový ventil + redukčný ventil PB
Famater - O tom se zde už před časem diskutovalo.
http://www.svarforum.cz/forum/viewtopic … 83#p149783
Offline
#90 23-01-2024 13:29:50
- Famater
- Člen
- Místo: Hradec Králové
- Registrovaný: 24-01-2012
- Příspěvky: 5036
Re: Fľašový ventil + redukčný ventil PB
Vidíš na mém příkladu co dělá staroba.
TP1500, KITin 170LA, JLT250 ACDC,vodní chlazení vl. výroby, hořák SR18, Binzel SR26 s pot., Plasma CUT55, autogen PB-kyslík
Křemíková 3fáz 200A vl. konstrukce
Offline
#91 23-01-2024 13:38:43
Re: Fľašový ventil + redukčný ventil PB
Famater napsal(a):
Vidíš na mém příkladu co dělá staroba.
Ale ne!!! ![]() Vy jste na tom dobře! Zde se to jen těžko zpětně dohledává. Ten Chemtan jsem "nezažil", asi přišel později, než abychom ho ve firmě i ve škole měli k dispozici... Ale vážně by mne zajímalo, zde doopravdy dosahuje vyšší teploty plamene, než acetylén.
Vy jste na tom dobře! Zde se to jen těžko zpětně dohledává. Ten Chemtan jsem "nezažil", asi přišel později, než abychom ho ve firmě i ve škole měli k dispozici... Ale vážně by mne zajímalo, zde doopravdy dosahuje vyšší teploty plamene, než acetylén.
Offline
#92 23-01-2024 13:44:17
- Famater
- Člen
- Místo: Hradec Králové
- Registrovaný: 24-01-2012
- Příspěvky: 5036
Re: Fľašový ventil + redukčný ventil PB
Také mě to připadlo také divné. Já jsem se o tom dověděl náhodou. Syn vyrábí luky a majitel této firmy je (nebo byl?) jeho zákazník. Tak se jednou o tom zmínil.
TP1500, KITin 170LA, JLT250 ACDC,vodní chlazení vl. výroby, hořák SR18, Binzel SR26 s pot., Plasma CUT55, autogen PB-kyslík
Křemíková 3fáz 200A vl. konstrukce
Offline
#93 23-01-2024 13:54:09
Re: Fľašový ventil + redukčný ventil PB
Offline
#94 23-01-2024 14:56:02
- Famater
- Člen
- Místo: Hradec Králové
- Registrovaný: 24-01-2012
- Příspěvky: 5036
Re: Fľašový ventil + redukčný ventil PB
pěkná souprava. Vezmeš a jdeš.
TP1500, KITin 170LA, JLT250 ACDC,vodní chlazení vl. výroby, hořák SR18, Binzel SR26 s pot., Plasma CUT55, autogen PB-kyslík
Křemíková 3fáz 200A vl. konstrukce
Offline
#95 23-01-2024 15:25:19
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Frank napsal(a):
Pane Radime, nezlobte se, ale to, co jste zde předvedl, je sice velice odborné, ale tak trochu zbytečné. O co se zde dohadujete? To, co zde píšete o ionizaci a titanu je přitažené za vlasy. U elektrod pro svařování má obal tyto vlastnosti a základní funkce:
No, já jsem to nahodil jen tak z hlavy, co si pamatuji a nechtělo se mi ty údaje někde hledat.
Jinak souhlasím s Vámi, že přímo na svařování tyto znalosti svářeč nepotřebuje, ale na druhé straně se mohou hodit, když má poznat nějaké nesmysly nebo když nějaký marketingový šmejd se ho snaží třeba obrat vnucováním nějaké "zázračné nové technologie".
Asi tak.
Chemtan asi bude mít nižší teplotu plamene. Neznám nějakou jinou běžnou sloučeninu, který by se dala v plynném stavu spalovat v hořáku s kyslíkem a na jednotku spalin, hmotnosti nebo objemu uvolňovala víc energie než acetylén.
Offline
#96 23-01-2024 15:43:27
Re: Fľašový ventil + redukčný ventil PB
Radim napsal(a):
případně ověřit na nějakých jednoduchých zkouškách.
musím se přidat ke kritikům Radime ![]()
ty plyny o kterých je řeč jsou obvykle nedostupné, když už tak 50l láhev a to si nikdo na nějakou zkoušku jen tak nekoupí. ![]()
Kdysi se zde řešil ten Chemtan. Doputovala ke mě 10kg láhev obdobná co je do ní plněn PB a taky propan do ještěrek. Cenu si nepamatuji. Zkoušel jsem s tím řezat železo, topilo to trochu víc než PB ale nijak extremě. Uplně stejného výsledku můžu dosáhnout nastavením většího nahřívacího plamene.
Přidat Bary nebo větší trysku, trysky větších průměrů mají i hubici větší vnitřní průměr = větší plamen.
Likvidace ocelových konstrukcí. Excelentní paliči železa. A nově také dřevorubci.
Plasmy. Přímočaré pily ocasky. Ruční orbitální pila (za studena). Utahováky. Sbíjecí kladiva. Plošiny. Jeřáby.
Vaření obalenou elektrodou (Lorch).
Práce ve vysokých výškách a v hlubokých hloubkách. Práce v jedovatých a výbušných atmosférách. Nic levného.
Offline
#97 23-01-2024 15:46:13
Re: Fľašový ventil + redukčný ventil PB
Radim - Ale jistě, já nepochybuji o Vašich znalostech, naopak. Snad se jen někdy každý nechtěně splete... ![]() S tímto, co jste napsal souhlasím bez výhrady!
S tímto, co jste napsal souhlasím bez výhrady!
"Chemtan asi bude mít nižší teplotu plamene. Neznám nějakou jinou běžnou sloučeninu, který by se dala v plynném stavu spalovat v hořáku s kyslíkem a na jednotku spalin, hmotnosti nebo objemu uvolňovala víc energie než acetylén."
Offline
#98 04-08-2025 20:02:23
- Avia_Furgon
- Člen

- Registrovaný: 04-05-2019
- Příspěvky: 22
Re: Fľašový ventil + redukčný ventil PB
HADICOVÁ RYCHLOSPOJKA PROPAN - BUTAN.
Zdravím a po delší době obnovuji diskusi.
Hadicová ROZDVOJKA na propan - butan zdárně vyřešena a ověřena praxí.
Nejprve obyčejnou mosaznou rozdvojkou "hvězdou".
Následně rozdvojkou uzavírací. Umožňuje práci jednoho či dvou izolatérů (čili jedna hadice nemusí být na rozdvojku při práci připojena).
Používám to i když pracuji sám v ploše a napojuji se v detailu na nějakou konstrukci. Zapojím si velký a střední hořák a při práci je střídám.
Ověřeno mnoha měsíci fungování.
No jo! Ale - nešlo by to ještě jednodušeji?
Co kdybych mohl mít jen JEDNU hadici a na jejím konci během práce měnil hořáky i s rukojetí? Tedy ne měnit samotný hořák před rukojetí (šroubovat převlečnou matici na prodlužovací trubce hořáku), ale měnit celý komplet rukojeť + prodlužovací trubka + hořák pomocí rychlospojky.
Má s tím někdo zkušenost?
Je to vhodné umístit na konec rukojeti (na vstupu PB do rukojeti)? Nebude se to nějak lámat, viklat, rozpojovat?
Je ta rychlospojka otočná? Lze protáčet připojenou rukojeť vůči hadici a nebude se hadice kroutit?
Rychlospojka se kupuje ve dvou kusech? Třeba v mém případě jeden konec na hadici a tři protikonce na tři rukojeti s hořáky?
Ď. za příp. odp.


A proč doprkýnka nefunguje vkládání obrázků? (Odkazy jsou funkční, pokud někoho bude bavit to kopírovat do adresního řádku.)
- - -
A hlavně: když tu rychlospojku pod tlakem rozpojím, uzavře se nějak? Nebo to z ní fučí pořád ven? To by pak bylo jaksi na nic...
Editoval Avia_Furgon (04-08-2025 20:22:35)
Offline
#99 04-08-2025 21:59:51
- Radim
- Člen
- Místo: Severní Morava
- Registrovaný: 17-12-2008
- Příspěvky: 4771
Re: Fľašový ventil + redukčný ventil PB
Zkoušel jsem, obrázky jdou normálně vkládat.
Editoval Radim (04-08-2025 22:05:04)
Offline
#100 04-08-2025 22:34:47
- Avia_Furgon
- Člen

- Registrovaný: 04-05-2019
- Příspěvky: 22
Re: Fľašový ventil + redukčný ventil PB
Pak nevím, kde dělám chybu?
Postupoval jsem podle návodu, vložil jsem do příspěvku tagy [img]a[/img].
Výsledek vidíš v mém přechozím příspěvku.
Ty obrázky na uvedených adresách existují. Ale zde se nezobrazují.
Prosím, můžeš zkusit napsat nějaký zkušební příspěvek a vložit tam tyto obrázky z uvedených odkazů? Jestli to půjde?
Děkuji.
Postupoval jsem tak v "Rychlé odpovědi".
Ještě to tedy zkusím v "Zaslat příspěvek".
Offline
- Index - hlavní stránka
- » Svařování plamenem a řezání kyslíkem
- » Fľašový ventil + redukčný ventil PB

